Li-Fraumeni sündroom ehk LFS on geneetiline seisund, mis soodustab inimesi mitmesuguste vähkide tekkeks. LFS-i põdevatel inimestel tekivad need vähid sageli varem kui kogu elanikkonnale tüüpiline. LFS-is võib olla ka suurem teine või järgnev vähk.
Seda sündroomi tuvastati esmakordselt mitmes peres, kus juba elu alguses tekkis mitmesuguseid erinevaid vähke, eriti sarkoome. Lisaks ilmnes, et pereliikmetel on elu jooksul tõenäolisemalt mitu uut ja erinevat vähki. Frederick Li ja Joseph Fraumeni Jr olid arstid, kes esmakordselt nendest avastustest teatasid 1969. aastal ja nii sai LFS oma nime.
Kangelaspildid / Getty ImagesMiks on suurem vähirisk?
Li-Fraumeni sündroomiga inimestel on suurem vähirisk, kuna nad on pärinud nn iduliini mutatsioonina olulises geenis, mida nimetatakseTP53.
Iduliini mutatsioon on geneetiline muutus, mis on toimunud mõjutatud indiviidi vanemate iduliinis - see tähendab, et algul esineb mutatsioon munasarjade või munandite rakkudes, mis põhjustavad muna ja sperma. Nendes rakkudes esinevad mutatsioonid on ainsad mutatsioonide liigid, mida saab eostamise ajal otse järglastele edasi anda, kui muna ja sperma kohtuvad sügootiks. Seega mõjutavad iduliini mutatsioonid uue järglase keha kõiki rakke; seevastu arenevad somaatilised mutatsioonid mingil hetkel indiviidispärastkontseptsiooni või palju, palju hiljem, ja need mõjutavad muutuvat arvu rakke kehas.
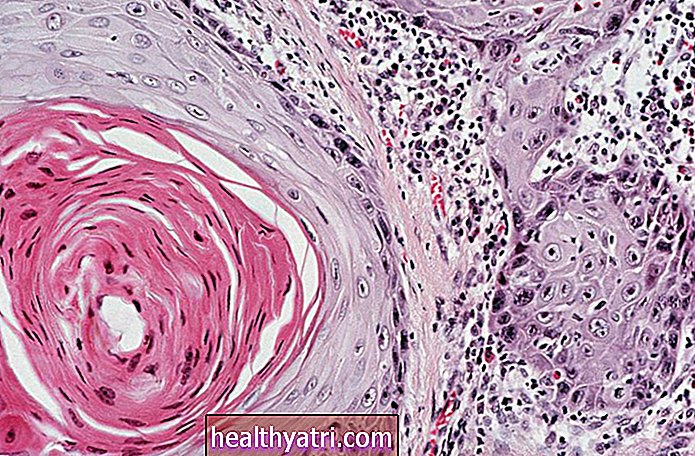
LFS-iga perekondade peamised iduliini mutatsioonid on need, mis mõjutavad LFS-i funktsiooniTP53geen. Vähiuuringute maailmas onTP53 geen on nii kriitiline, et seda on nimetatud "genoomi valvuriks".
TP53 on kasvajat pärssiv geen - see tähendab, et see on geen, mis kaitseb rakku ühe sammu juurest vähini. Kui see geen muteerub nii, et see ei toimi nii, nagu on ette nähtud, või et selle funktsioon oleks oluliselt vähenenud, võib rakk vähktõveks areneda, sageli koos teiste geneetiliste muutustega. TestimineTP53 iduliini mutatsioonid töötati esmakordselt välja 1990. aastal, kui seos p53 ja LFS vahel kinnitati. Sellest ajast alates on kogu maailmas peaaegu 250 mutatsiooniTP53 geen on tuvastatud.
LFS-iga on seostatud ka mutatsiooni teises geenis, hCHK2; selle tähendus on siiski ebaselge. HCHK2 geen on kasvajat pärssiv geen, mis aktiveerub vastusena DNA kahjustusele. Seda mutatsiooni kannavad ainult vähesed pered ja kannatanutel on pahaloomuliste kasvajate vahemik sarnane TP53 mutatsioonidega perekondadele.
Kui suur on risk?
Hinnanguliselt on LFS-iga inimesel 40-aastaselt vähktõve tekkimise tõenäosus 50% ja 60-aastaseks saamise tõenäosus 90%. Kui teil on LFS, sõltub teie individuaalne risk osaliselt kas olete mees või naine, emastel on tavaliselt suurem risk kui meestel.
Kui vaadata 50-aastaselt LFS-iga meeste ja naiste eluaegset vähiriski, siis vähktõve tekkimise risk jaguneb järgmiselt: naistel 93% ja meestel 68%. Kui neil vähk areneb, kipuvad naised seda vähki haigestuma ka varasemas eas: keskmiselt 29 aastat, meestel 40 aastat.
Naiste suurem risk on peamiselt tingitud varakult algavast rinnavähist, selgub Mai ja tema kolleegide uuringust. Need teadlased leidsid ka, et nende naiste seas, kellel oli positiivne tulemusTP53mutatsioonid, oli rinnavähk ülekaalukalt kõige levinum pahaloomuline kasvaja. Kumulatiivne rinnavähi esinemissagedus oli 60-aastaselt umbes 85%. Samas uuringus suurenes rinnavähi risk naise 20ndates eluaastates, mis kinnitas, et 20-aastastelt algav rinnavähi sõeluuring on hea tava LFS-iga naistel.
See riskitaseTP53mutatsioonid on võrreldavad emastel, kellel on iduliini mutatsioonid BRCA1 ja BRCA2 - geenid, mis tõusid esile BRCA1 / 2 mutatsioonide ja ennetavate mastektoomiate geneetilise testimise meediumide aruannetes (kuulsused, näiteks Angelina Jolie).
Millega on seotud põhilised vähid?
Iga vähk võib areneda igal inimesel igal ajal. Siiski on teada, et LFS-iga inimestel on varajane vähidiagnoos ja neil on kogu elu jooksul suur hulk vähivorme, sealhulgas järgmine:
- Osteosarkoom - kõige levinum vähivorm, mis algab luudest
- Pehmete kudede sarkoomid - teatud tüüpi vähk, mis areneb teatud kudedest, nagu rasv, lihased, närvid, kiudkuded, veresooned või sügavad nahakuded
- Varakult algav rinnavähk
- Ajukasvajad
- Leukeemia - vererakkude vähk
- Neerupealiste koore kartsinoom - neerupealise koore vähk, mis on neerupealiste välimine kiht (neerupealised asuvad neerude peal ja neil on oluline roll mitmesuguste hormonaalsete funktsioonide korral)
1997. aastal Kleihues'i uuringus oli LFS-is kõige sagedamini tuvastatud sarkoom osteosarkoom, mis vastas 12,6% juhtudest, millele järgnesid ajukasvajad (12%) ja pehmete kudede sarkoomid (11,6%). Pehmete kudede sarkoomidest tuvastati kõige sagedamini rabdomüosarkoome. Teiste, harvemini esinenud sarkoomide hulka kuuluvad fibrosarkoomid (mida ei peeta enam tõeliseks üksuseks), ebatüüpilised fibroksantoomid, leiomüosarkoomid, orbitaalsed liposarkoomid, spindlirakkude sarkoomid ja diferentseerumatud pleomorfsed sarkoomid. Hematoloogilised kasvajad või verevähid (näiteks äge lümfoblastiline leukeemia ja Hodgkini lümfoom) ja neerupealiste koore kartsinoomid esinesid vastavalt 4,2% ja 3,6%.
Kuna on tuvastatud rohkem perekondi, kellel on LFS-ile tüüpilised geneetilised mutatsioonid, on sellega seotud palju rohkem vähke.
LFS-i vähi spekter on laienenud, hõlmates melanoomi, kopsu, seedetrakti, kilpnäärme, munasarjade ja muid vähke.
Traditsiooniliste hinnangute põhjal näib pehmete kudede sarkoomi ja ajuvähi tekkimise oht olevat suurim lapsepõlves, samas kui osteosarkoomi risk võib olla kõige suurem noorukieas ja naissoost rinnavähi risk suureneb märkimisväärselt umbes 20-aastaselt ja jätkub vanemaks täiskasvanuks saamine. See statistika võib siiski muutuda, kuna vähi eelsoodumusega geenide testimise tavad on arenenud.
Kuidas määratakse Li-Fraumeni sündroom?
Selle sündroomi jaoks on erinevad kriteeriumid ja määratlused. Mõned on kaasavamad kui teised. Klassikaline LFS on kõige piiravam määratlus, kuna see nõuab sarkoomidiagnoosi enne 45. eluaastat, samas kui järgnevad määratlused, näiteks Chompreti kriteeriumid, püüavad diagnoosi andmisel rakendada arenevat teaduslikku teavet kasvaja tüüpide ja vanuse kohta.
Klassikalised LFS-i kriteeriumid:
- Teil diagnoositakse sarkoom (vähitüüp, mis hõlmab lihase / skeleti / liigeste / rasva päritolu rakke) enne 45-aastast
- Las teil on esimese astme sugulane (vanem, õde-vend või laps), kellel on diagnoositud vähk enne 45-aastast ja vanemat vanust
- Kas teil on mõni muu esimese või teise astme sugulane (sealhulgas tädid, onud jt), kellel on vähk, mis on diagnoositud enne 45-aastast või sarkoom, mis on diagnoositud igas vanuses.
Li-Fraumeni-laadsed (LFL) kriteeriumid:
- LFL-i kriteeriumid hõlmavad laiemat võrku, hõlmates muid vähitüüpe ja hõlmates mõnda sugulast, kellel diagnoositakse pärast 45-aastast vanust, ja kasutusel on kaks erinevat määratlust:
- Kase määratlus: teil on diagnoositud mis tahes lapsepõlves esinev vähk või sarkoom, ajukasvaja või neerupealiste kartsinoom, mis on diagnoositud enne 45-aastaseks saamist ja teil on esimese või teise astme sugulane tüüpilise Li-Fraumeni vähiga (sarkoom, rinnavähk, ajukasvaja, adrenokortikaalne kartsinoom või leukeemia) igas vanuses ja kellel on esimese või teise astme sugulane vähiga enne 60-aastast.
- Angerja määratlus: teil on igas vanuses kaks esimese või teise astme sugulast, kellel on Li-Fraumeni seotud pahaloomulised kasvajad (sarkoom, rinnavähk, ajukasvaja, leukeemia, neerupealiste kortikaalne kasvaja, melanoom, eesnäärmevähk, kõhunäärmevähk).
Kriteeriumid:
- Teil on enne 46-aastast vananemist Li-Fraumeni kasvaja spektrisse kuuluv kasvaja (pehmete kudede sarkoom, osteosarkoom, menopausieelne rinnavähk, ajukasvaja, neerupealiste kortikaalne kartsinoom, leukeemia või bronhoalveolaarne kopsuvähk) ja teil on vähemalt üks esimese või teise - kraadiga sugulane, kellel on Li-Fraumeni kasvaja (välja arvatud rinnavähk, kui teil on rinnavähk) enne 56-aastast või mitme kasvajaga või
- Teil on mitu kasvajat (välja arvatud mitu rinnakasvajat), millest kaks kuuluvad Li-Fraumeni kasvaja spektrisse ja esimene neist ilmnes enne 46-aastast või vanemat
- Teil diagnoositakse adrenokortikaalne kartsinoom või soonkesta kasvaja, sõltumata perekonna ajaloost.
Vastavalt Schneideri ja tema kolleegide LFS-i ülevaatele on vähemalt 70% kliiniliselt diagnoositud isikutest (st kasutades ülaltoodud definitsioone) tuvastatav kahjulik iduliini mutatsioonTP53kasvajat pärssiv geen.
Vähktõve juhtimine
Kui LFS-iga isikul tekib vähk, on soovitatav rutiinne vähiravi, välja arvatud rinnavähk, kus teise rinnavähi riskide vähendamiseks ja kiiritusravi vältimiseks on soovitatav mitte lumpektoomia, vaid mastektoomia.
LFS-iga põdevatel inimestel soovitatakse võimaluse korral vältida kiiritusravi, et vähendada sekundaarsest kiirgusest põhjustatud pahaloomuliste kasvajate riski. Kui aga kiiritust peetakse meditsiiniliselt vajalikuks, et parandada antud pahaloomulise kasvaja korral ellujäämise võimalust, võib seda kasutada raviarsti ja patsiendi äranägemisel.
Sõelumine ja jälgimine
Ekspertidelt on üha enam kutsutud üles saavutama üksmeelt selles osas, kuidas FLS-iga peresid tuleks läbi vaadata ja hoolitseda. Kuigi teadus areneb kiiresti, puudub kahjuks selline konsensus kõigis valdkondades.
Kahjulike esinemissagedusTP53 mutatsioonid üldpopulatsioonis pole teada ja FLSi tegelik sagedus pole teada. Hinnangud varieeruvad vahemikus 1 000 kuni 1 000 000. Mida rohkem peresid läbibTP53testimisel võib LFS-i tegelik levimus selgemaks saada.
Rinnavähi riski käsitlemine
Ameerika Ühendriikides soovitatakse riikliku üldise vähivõrgustiku (National Comprehensive Cancer Network, NCCN) suunistes iga-aastast rindade MRI-d neile, kellel on FLS vanuses 20–29 aastat ning iga-aastane MRI ja mammograafia vahemikus 30–75 aastat. Austraalias soovitatakse riiklikes suunistes pakkuda kahepoolset mastektoomiat; muul juhul on iga-aastane rinnanäärme MRI soovitatav vahemikus 20-50 aastat. Schon ja tema kolleegid soovitavad kaaluda riski vähendava kahepoolse mastektoomia või rindade skriinimise võimalust naistel, kellel pole vähki ja kellel on mutatsioonTP53 geen.
NCCN soovitused
Tuginedes järeldusele, et rinnavähi risk suureneb pärast teist kümnendit märkimisväärselt, on soovitused sisaldanud kahepoolse mastektoomia arvestamist alates 20. eluaastast. Rinnavähi aastane riskitipp saabub umbes 40–45-aastaselt ja seejärel väheneb, nii et kahepoolne mastektoomia on vähem kasu üle 60-aastastele naistele.
- Rindade teadlikkus alates 18. eluaastast, perioodiline ja järjepidev rindade enesekontroll.
- Kliiniline rindade eksam iga 6–12 kuu järel, alates 20. eluaastast
- Vanus 20–29 aastat, iga-aastane rindade MRI skriining kontrastiga
- Vanus 30–75 aastat, iga-aastane rindade MRI skriining kontrastsuse ja mammogrammiga, arvestades Tomosünteesi
- Vanus> 75 aastat, juhtimist tuleks kaaluda individuaalselt.
- Naistele, kellel on aTP53rinnanäärmevähi ravis ja kellel pole olnud kahepoolset mastektoomiat, tuleb sõeluuringud iga-aastase rinnanäärme MRI ja mammogrammiga jätkata, nagu eespool kirjeldatud.
- Kui arutatakse riski vähendava mastektoomia võimalust, peaks olema nõu kaitse taseme, vanusespetsiifilise vähiriski, rekonstrueerimisvõimaluste ja teiste vähktõvega konkureerivate riskide osas. Sellistesse aruteludesse tuleks kaasata riski vähendava mastektoomia psühhosotsiaalsed, sotsiaalsed ja elukvaliteedi aspektid.
Muu vähiriski käsitlemine
NCCN soovitused
- Põhjalik füüsiline eksam, sealhulgas neuroloogiline läbivaatus kõrge kahtlusnäitajaga harvaesinevate vähkide ja teiste pahaloomuliste kasvajate osas vähist ellujäänutel iga 6–12 kuu järel.
- Kolonoskoopia ja ülemine endoskoopia iga 2–5 aasta tagant, alustades vanusest 25 aastat või 5 aastat enne perekonna teadaolevat kõige varasemat käärsoolevähki (olenevalt sellest, kumb saabub varem).
- Iga-aastane dermatoloogiline uuring algab 18 aastast.
- Iga-aastane kogu keha MRI
- Iga-aastast aju MRI võib teha kogu keha MRI osana või eraldi eksamina.
Muud skriiningu ja järelevalve vormid
LFS-iga täiskasvanutel viidi läbi positronemissioontomograafia (FDG-PET) / CT-uuringute pilootkatse, mis tuvastas kasvajad 15 isikul kolmel. Need PET-CT skannid, kuigi sobivad teatud kasvajate leidmiseks, suurendavad ka iga kord, kui neid tehakse, kiiritust, mistõttu see skaneerimismeetod peatati ja on üle läinud kogu keha MRT-le täiskasvanuteleTP53kahjulikud variandid.
Mitmed uurimisrühmad on hakanud kasutama intensiivset skriiningprogrammi, mis hõlmab kogu keha kiiret MRT, aju MRI, kõhuõõne ultraheliuuringut ja neerupealiste koore funktsiooni laborikatseid. Selline seireprogramm võib parandada LFS-iga inimeste ellujäämist, tuvastades kasvajad enne sümptomite ilmnemist, kuid on vaja rohkem uuringuid, et näidata, et selline režiim töötab LFS-iga täiskasvanutel ja lastel.
LFS-iga inimestelt on küsitud nende suhtumise kohta vähijälgimisse ja enamik näib uskuvat järelevalve väärtusesse kasvajate varases staadiumis avastamiseks. Nad teatasid ka kontrolli- ja turvatundest, mis on seotud osalemisega tavalises seireprogrammis.
Laste testimine TP53 mutatsioonide suhtes
Lapsi ja noorukeid on võimalik testida LFS-i iseloomulike mutatsioonide osas, kuid on tõstatatud küsimusi selle võimalike riskide, eeliste ja piirangute kohta, sealhulgas tõestatud järelevalve- või ennetusstrateegiate puudumine ning mured stigmatiseerimise ja diskrimineerimise pärast.
Alla 18-aastaseid isikuid on soovitatav testidaTP53 patogeenseid variante saab teha programmi raames, mis pakub nii testieelset kui ka -järgset teavet ja nõustamist.



-to-prevent-breast-cancer-recurrence.jpg)