Meie immuunsüsteem on tõelised imed - need hoiavad meie kubisevaid soolebaktereid kontrolli all; nad võitlevad sissetungivate viiruste paisuga ja likvideerivad edukalt suurema osa vähkidest juba ammu enne, kui neist kunagi probleemiks saab. Olulised avastused immunoteraapia valdkonnas on viimase 20 aasta jooksul viinud märkimisväärsete uute arenguteni ravimeetodites, mis veelgi parandavad immuunsüsteemi funktsioone.
Kangelaspildid / Getty ImagesImmunoteraapia areng
Enne eesnäärmevähi immunoteraapia võimaluste ülevaatamist pange tähele, et tõhusa immunoteraapia teel on olnud palju valesid alustamisi ja enneaegseid võidudeklaratsioone. Näiteks kinnitas FDA 20 aastat tagasi melanoomi jaoks interleukiin 2. Vaatamata ainult 10% -lise ravivastuse määrale ja tugevalt toksilisele toimele pakkus interleukiin 2 lootust ajal, mil metastaatiline melanoom oli täiesti lootusetu ja ravimatu. Ravim oli väike, kuid lootustandev tulevase, tõhusama teraapia julgustus.
Nüüd kuuleme dramaatilisi pöördeid melanoomi ravis. Näiteks käskis meedia meil hiljuti valmistuda president Jimmy Carteri lõpuks - tema melanoom oli levinud ajju. Siis oli näiline ime - uus immunoteraapia ravim - muutnud ta vähivabaks. Kaasaegne immunoteraapia võib lootusetud juhtumid muuta remissiooniks.
Kuidas on toimunud radikaalne areng? Immuunsüsteemi sisemise töö mõistmises on tohutult süvenenud. Lihtsamalt öeldes teame nüüd, et immuunsüsteem koosneb kolmest põhikomponendist:
- Reguleerivad rakud, mida nimetatakse TReg-deks, hoiavad immuunsüsteemi üliaktiivsuse kontrolli alt väljumast.
- Killer-T rakud ründavad vähirakke ja tapavad neid.
- Dendriitrakud töötavad detektorrakkudena, tuhandavad vähi ja leiavad selle ning suunavad seejärel immuunsüsteemi, et see teaks, milliseid rakke hävitada. Pärast vähi avastamist suunavad dendriitrakud mõrvarakud vähki koju elama ja ründavad vähki.
Kättemaks eesnäärmevähi eest
Kui FDA 2010. aastal Provenge heaks kiitis, oli eesnäärmevähk immuunparteis suhteliselt varajane osaleja. FDA heakskiit põhines randomiseeritud, topeltpimedas, platseebokontrolliga kliinilises uuringus, mis näitas suhtelise riski olemasolu Provenge-ravi saanud patsientide surmaohu vähenemine 22%, mis oli seotud keskmise elulemuse 4-kuulise paranemisega võrreldes platseebogrupiga.
Provenge töötab uudse meetodiga, mis suurendab dendriitrakkude aktiivsust. Nagu varem märgitud, on dendriitrakud immuunsüsteemi "verekoerad", mis on võimelised vähirakke nuuskima ja leidma. Provenge'i protsess põhineb dendriitrakkude eemaldamisel vere ekstraheerimisel leukafereesiga. Seejärel töödeldakse neid rakke laboris, mis võimaldab neil ära tunda eesnäärmevähi fosfataasi (PAP) - tavalist molekulaarset tunnust, mis asub eesnäärmevähirakkude pinnal. Pärast aktiveerimist infundeeritakse dendriitrakud patsiendi verre, kus nad stimuleerivad tapja T-rakke vähirakkude paremaks tuvastamiseks ja rünnakuks, kuna neil on võimaldatud tuvastada PAP-pinna funktsioon ja kasutada seda sihtmärgina.
Provenge’i võib pidada isikupärastatud vähiteraapia ülimaks, kuna dendriitrakud filtreeritakse iga patsiendi verest, suurendatakse laboris eesnäärmevähirakkude rünnakuks ja seejärel infundeeritakse uuesti samale patsiendile. Nii põnev kui see tehnoloogia kõlab, võib olla üllatav kuulda, et arstid ja patsiendid on Provenge'i kasutamise ideele aeglaselt soojenenud. See loid suhtumine Provenge'i omaksvõtmisse oli ootamatu, kui Provenge esmakordselt turule tuli, arvestades paljude immuunsust parandavate alternatiivsete ravimeetodite, nagu Graviola, shiitake seened, pau de arco ja Essiac tee, populaarsust. Miks peaks FDA heakskiidetud tüüpi immuunravi kasutamisel olema kõhklusi?
Kriitika
Kriitikud tõid välja, et Provenge on kallis ja keskmine saaja elab vaid kolm või neli kuud rohkem. Vähiravi reaalses maailmas (mitte kliiniliste uuringute maailmas) on see vale oletus. Kliinilistes uuringutes osalevad mehed ei ole tüüpilised eesnäärmevähiga patsiendid, kes saavad FDA heakskiidetud ravimeetodeid. Üldiselt on kliinilistes uuringutes osalevatel meestel haigus palju arenenum. Seda seetõttu, et patsiendid viivitavad kliinilises uuringus osalemisega seni, kuni standardravi ebaõnnestub.
Seetõttu kipub meeste ellujäämine kliinilises uuringus olema suhteliselt lühike, olenemata kasutatava ravi tüübist. Sellest hoolimata peavad kõik ebasoodsates tingimustes ellujäämist pikendavad ravimid olema tagajärjed. Seetõttu saavad ravimid, millel on elulemuse pikenemine, FDA heakskiidu. Asi on selles, et ravim näitab paremaid tulemusi, kui seda kasutatakse meeste varasemas etapis.
Ravi erinevatel etappidel
Eeldust, et Provenge'il on suurem mõju, kui seda kasutatakse eesnäärmevähi raviks varasemas staadiumis, uuriti algandmete uuesti analüüsimise kaudu, mis viis FDA Provenge'i esialgse heakskiiduni. Kordusanalüüs näitas, et varases staadiumis haigusega meestel oli ellujäämise pikenemine tõepoolest palju suurem. Tegelikult muutus ellujäämise pikenemine järk-järgult suuremaks, kui Provenge'i hakati varem alustama.
Selles reanalüüsis hinnati nelja meestegruppi, kes olid jaotatud nende erinevate PSA tasemete järgi Provenge-ravi alguses: mehed, kelle PSA tase oli alla 22, mehed, kellel PSA oli vahemikus 22 kuni 50, mehed, kellel PSA oli vahemikus 50 kuni 134, ja mehed PSA-ga üle 134.
Allolevas tabelis on kokku võetud Provenge'iga ravitud meeste elulemus võrreldes platseeboga ravitud meestega, jagatuna PSA tasemega Provenge'i alguses. Provenge'i ja platseebo netoelulemuste erinevus (kuudes) on loetletud viimasena.
PSA tase
≤22
22–50
50–134
>134
Patsientide arv
128
128
128
128
Kättemaks
41.3
27.1
20.4
18.4
Platseebo
28.3
20.1
15.0
15.6
Ellujäämise erinevus
13.0
7.1
5.4
2.8
Nagu tabel illustreerib, oli ellujäämise eelis kõigil Provenge'iga ravitud rühmadel võrreldes platseeboga ravitud meestega. Ellujäämise paranemine oli aga kõige suurem meestel, kes alustasid Provenge'i siis, kui PSA oli kõige madalam. Mehed, kes alustasid Provenge'i, kui nende PSA oli alla 22-aastane, elasid 13 kuud kauem kui sarnases staadiumis platseebot saanud mehed. Väga kaugelearenenud staadiumis mehed, kelle PSA tase oli üle 134, elasid vaid mõni kuu kauem kui mehed, kes said platseebot.
Rakendus
Naysayers kahtleb Provenge'i efektiivsuses mõnel muul põhjusel. Enamik efektiivse eesnäärmeteraapia tüüpe, näiteks hormoonravi ja keemiaravi, põhjustavad PSA taseme langust. Kuid Provenge puhul see tavaliselt nii ei ole. Inimesed mõtlevad seetõttu, kuidas saab Provenge pikendada ellujäämist?
Nad unustavad, et tavaliste eesnäärmevähi ravimeetodite, nagu kemoteraapia ja hormoonide blokaad, efektiivsus püsib ainult pideva rakendamise abil. Kui ravi on lõpetatud, vähivastane toime lakkab ja vähk jätkab kasvu.
Seevastu immuunsüsteemil, kui see on aktiveeritud, on püsiv ja pidev toime. Seega, isegi kui Provenge põhjustab haiguse progresseerumisel ainult minimaalset aeglustumist, kuna toime on pidev, avaldub kumulatiivne toime patsiendi ülejäänud elu jooksul. Ja mida kauem mees elab, seda suurem on kasu suurus.
Vähi metastaaside jälgimine
Ülaltoodud tabelis esitatud andmete põhjal järeldatakse loogiliselt, et Provenge'i tuleb alustada kohe kõigil meestel, kellel on diagnoositud kliiniliselt oluline eesnäärmevähk. Kahjuks katavad kindlustusseltsid Provenge'i ravi alles pärast seda, kui meestel tekib hormoonide (Lupron) resistentsus ja vähi metastaasid. Kuna enamikul juhtudel tekib hormoonresistentsus enne metastaase, peaksid taastuva eesnäärmevähiga mehed, kes kontrollivad oma PSA-d Luproniga, jälgima PSA tõusu. Hormooniresistentsus on määratletud kui PSA tõus Luproni või mis tahes Luproni-laadse ravimi kasutamisel.
Esimesel näidustusel, et PSA hakkab tõusma, peaksid mehed alustama metastaaside jõulist otsimist. Praegu on PET-uuringud parim viis metastaaside leidmiseks, kui PSA on endiselt suhteliselt madalas vahemikus, näiteks kahe all. PET-i skaneerimise kasutamist võib kaaluda mitut tüüpi: F18 luu skaneerimine, Axumin, C11 atsetaat, C11 koliin või Gallium68 PSMA. Kui nende uuringutega ei õnnestu metastaatilist haigust esialgu tuvastada, tuleb neid korrata vähemalt iga kuue kuu tagant, kuni metastaatiline haigus leitakse, pärast mida tuleb Provenge kiiresti alustada.
Teine immunoteraapia tüüp
Viimase 30 aasta jooksul on paljud katsed immuunsüsteemi rakendada ebaõnnestunud. Me hakkame õppima, et need tõrked on tingitud immuunsüsteemi regulatiivse komponendi liigsest aktiivsusest. Alati, kui keha tekitab uut immuunaktiivsust, stimuleerib see aktiivsus iseregulatsiooni kasvava immuunvastuse summutamiseks. Selle eesmärk on vältida selliste destruktiivsete immuunhaiguste arengut nagu luupus, reumatoidartriit või hulgiskleroos.
Nüüd on teadlased teada saanud, et vähirakud kasutavad seda immuunsüsteemi regulatiivset komponenti, tootes immuunsust pärssivaid hormoone. Need hormoonid panevad immuunsüsteemi magama, võimaldades seeläbi vähirakkudel paljuneda, hoides tapja T-rakke eemal. Reguleerivad rakud, Tregi rakud, on teatud mõttes "röövitud" ja neid kasutatakse kilbina, et vähendada meie immuunsüsteemi vähivastast toimet. See immuunsüsteemi võimetus vähki rünnata ei tulene immuunsuse nõrkusest; pigem on see vähirakkude tekitatud immuunsuse pärssimine suurenenud regulatiivse aktiivsuse tõttu. Selle uue arusaama kohaselt on selle probleemi kompenseerimiseks välja töötatud spetsiifilised farmatseutilised ained.
Yervoy on selline ravim, mis on FDA poolt heaks kiidetud melanoomi raviks. Yervoy toimib blokeerides TLA-efektori ja Tregi rakkude pinnal oleva reguleeriva lüliti CTLA-4. Kui see lüliti on sisse lülitatud, suureneb regulatiivne aktiivsus ja immuunsus pärsitakse. Kui Yervoy lülitab CTLA-4 välja, lülituvad T-efektorrakud aktiivseks, Tregi rakkude inhibeeriv toime pärsitakse ja netoefekt suurendab immuunsüsteemi aktiivsust.
Esialgsed uuringud, milles hinnati Yervoy't eesnäärmevähiga meestel, näitavad lubadust, eriti kui see on kombineeritud kiiritusega (vt allpool). Kuid uuemad uuringud näitavad, et teine regulatsiooni blokeeriv ravim nimega Keytruda võib paremini töötada.
Keytruda blokeerib teise regulatiivse lüliti PD-1. Esialgsed uuringud eesnäärmevähiga patsientidel viitavad sellele, et Keytruda võib põhjustada suuremat vähivastast toimet kui Yervoy ja põhjustada vähem kõrvaltoimeid. Kui need esialgsed leiud Keytrudaga kinnitatakse, võib kombineeritud ravi Keytruda ja Provenge'iga olla hea viis immuunsüsteemi vähivastase toime veelgi tugevdamiseks.
Abskopaalne efekt
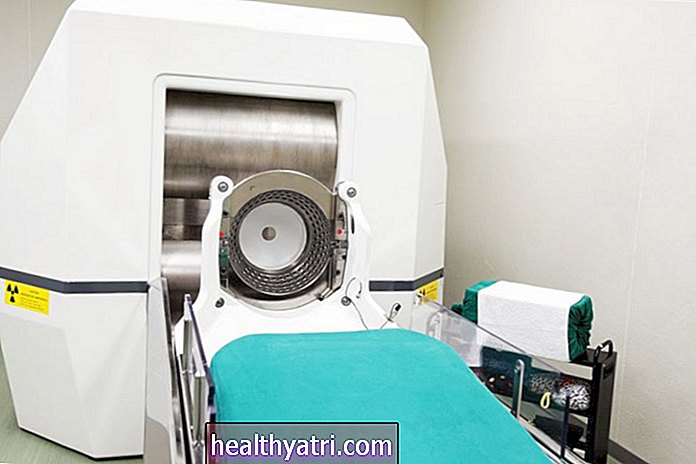
Kiirgus, mis on suunatud skaneeringuga tuvastatud metastaatilisele kasvajale, on veel üks potentsiaalne viis immuunsüsteemi stimuleerimiseks protsessi kaudu, mida nimetatakse Abscopali efektiks. Kui kiirgusvihk kahjustab kasvajarakke, lähenevad meie immuunsüsteemi rakud surevale kasvajale ja eemaldavad järelejäänud rakujäägid. Abscopal-efekt seisneb seetõttu selles, et immuunrakud tuvastavad kõigepealt kasvajaspetsiifilised molekulid surevatel kasvajarakkudel ja seejärel jahtivad vähirakke teistes kehaosades, kasutades märklaudana neid samu kasvajaspetsiifilisi molekule.
Kiirgusest põhjustatud immuunteraapial on mitu atraktiivset aspekti:
- Valikuliselt ja oskuslikult manustamisel ei esine kõrvaltoimeid.
- Ravi on kaetud kõigi kindlustusvormidega.
- Kiirgus on tavaliselt piisavalt tugev sihtmärgiks oleva kasvaja kõrvaldamiseks.
- Kohtkiirgust on lihtne kombineerida Provenge, Keytruda või mõlemaga.
Sõna Verywellist
Meie arusaam eesnäärmevähi immuunteraapiast areneb kiiresti, kuid on alles lapsekingades. Sellegipoolest on põnev tõdeda, et meie käsutuses on juba mitu tõhusat tööriista. Edasine väljakutse on õppida, kuidas neid uusi tööriistu saab kasutada optimaalselt, kas ise või koos. Hoidke oma arstiga avatud vestlust immunoteraapia võimaluste kohta, et teha kindlaks, kas need sobivad teile.























.jpg)