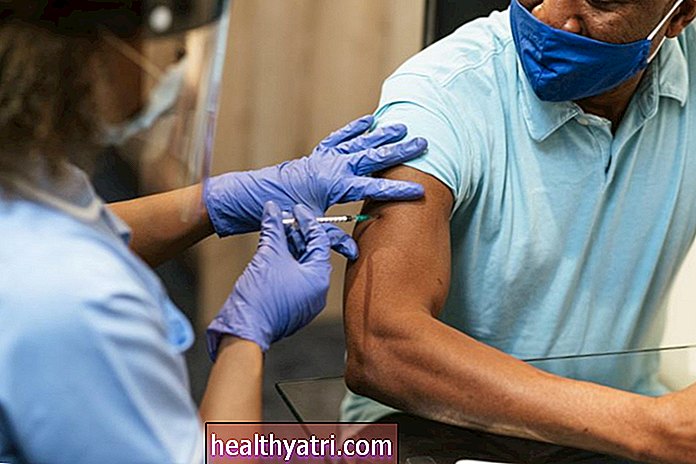
Sasiistock / Getty Images
Võtmed kaasa
- Pfizer on saanud FDA heakskiidu koroonaviiruse vaktsiini testimise alustamiseks 12-aastastel ja vanematel lastel.
- Eksperdid ütlevad, et laste kaasamine kliinilistesse uuringutesse on ülitähtis vaktsiini üldise väljatöötamise jaoks, mis kaitseb nii lapsi kui ka täiskasvanuid COVID-19 eest.
- Oma veebisaidi andmetel on Pfizer oma uuringusse kaasanud juba üle 39 000 vabatahtliku. Üle 34 000 neist vabatahtlikest on juba saanud teise vaktsineerimise.
Ameerika Ühendriikide farmaatsiaettevõte Pfizer teatas oktoobris, et on saanud USA Toidu- ja Ravimiametilt (FDA) loa alustada 12-aastaste laste registreerimist oma koroonaviiruse vaktsiinikatsetes.
"Nii toimides saame paremini mõista vaktsiini võimalikku ohutust ja efektiivsust rohkem vanuses ja taustaga isikutel," ütles ettevõte ajakohastatud avalduses.
See on esimene COVID-19 vaktsiinikatsetus USA-s, mis hõlmab lapsi. Alates oktoobrist on Pfizer üks neljast USA ettevõttest, kellel on vaktsiinid 3. faasi kliinilistes uuringutes.
Pfizer oli juba laiendanud oma uuringu 3. faasi, hõlmates 16-aastaseid ja vanemaid lapsi, samuti inimesi, kellel oli krooniline, stabiilne inimese immuunpuudulikkuse viirus (HIV), C-hepatiit ja B-hepatiit.
Miks testida lastel COVID-19 vaktsiini?
Enne kui Pfizer sai heakskiidu lastega testimise alustamiseks, avaldasid eksperdid ajakirjas aruandeKliinilised nakkushaigusedmärkides sellise testimise olulisust.
"COVID-19 otsene mõju lastele on suurem kui mitmete teiste patogeenide puhul, mille jaoks meil on nüüd tõhusad lastevaktsiinid," märgitakse aruandes. „Lisaks on selgelt alahinnatud laste rolli SARS-CoV-2 edastamisel. Hoolikalt läbi viidud 2. faasi kliinilised uuringud võimaldavad adekvaatselt lahendada võimalikke COVID-19 vaktsiini ohutusprobleeme. "
Suzanne Pham, MD
Me ei saa selle viiruse levikust üle ega ümber, kui me oma lapsi vaktsineerime.
- Suzanne Pham, MDNew Yorgi Stony Brooki lastehaigla laste nakkushaiguste osakonna juhataja Sharon Nachman nõustub raportiga, öeldes Verywellile, et „lastearstid on väga huvitatud uuringu üksikasjade vaatamisest ja sellest, kuidas vaktsiin lastel toimib. . ”
Nachmani sõnul on vaktsiini katsetamisel lastel spetsiifilisi eeliseid. Teadlased saavad hinnata lühi- ja pikaajalist immuunvastust, mis hõlmab välja selgitamist, kas täiskasvanutel kasutatav vaktsiini doos on vajalik lastele või on neil madalama annusega sarnane immuunvastus.
Nachmani sõnul on samuti oluline märkida, et kuna täiskasvanute koronaviirusele võib eelneda kokkupuude lastel asümptomaatilise infektsiooniga, võib kogu pere ravimiseks mõeldud vaktsiini loomine „kodu- ja kogukondade leviku vähendamiseks palju ära teha”.
Suzanne Pham, MD, Chicago Weissi mälestushaigla peaarst, ütleb Verywellile, et mida varem saab lapsi vaktsineerida, seda varem väheneb ülekandekiirus.
"Laste efektiivse vaktsineerimisega väheneb oht, et lapsed viirust levitavad kogukonnas, eriti nende kõrge riskiga inimeste puhul, kes on raskete või kriitiliste haiguste suhtes vastuvõtlikumad," ütleb Pham Verywellile. „See võimaldab koolidel taasavamist alustada ja meie laste arenguks üliolulised tegevused jätkuvad kontrollitult. Me ei saa selle viiruse levikust jagu, kui me oma lapsi vaktsineerime. Meil peab olema piisavalt karja immuunsust ühiskonnas, et oleks võimalik levikut takistada. "
COVID-19 vaktsiinid: hoidke end kursis saadaolevate vaktsiinidega, kes neid saab ja kui ohutud nad on.
Kuidas vaktsiini proovid algavad?
Pham selgitab, et vaktsiini testimiseks - täiskasvanutel või lastel - peab ettevõte esitama FDA-le uue uuritava ravimi (IND) taotluse.
Rakenduses kirjeldatakse vaktsiini, selle valmistamise viisi ja kvaliteedikontrolli katseid. Taotlus sisaldab ka loomkatsete andmeid, mis näitavad, et vaktsiin on inimestel esmaseks katsetamiseks ohutu.
Nagu FDA selgitab, on taotlusprotsessil mitu sammu:
Uue ravimi varajase prekliinilise väljatöötamise ajal on sponsori peamine eesmärk välja selgitada, kas toode on inimestel esmakordseks kasutamiseks piisavalt ohutu ja kas ühendil on farmakoloogiline aktiivsus, mis õigustab kaubanduslikku arengut.
Kui toode on välja töötatud elujõulise kandidaadina edasiarendamiseks, keskendub sponsor seejärel andmete ja teabe kogumisele, mis on vajalik selleks, et tuvastada, et toode ei põhjusta inimestele piiratud algusjärgus kliinilistes uuringutes põhjendamatuid riske.
Seejärel läbivad vaktsiin 1. faasi uuringud, mis Phami selgitusel on "ohutuse ja immunogeensuse uuringud, mida tehakse vähese hulga hoolikalt jälgitavate inimestega".
"2. etapp koosneb doosivahemikuga uuringutest ja seda laiendatakse suurema hulga (sadade) inimesteni," ütleb Pham. "Seejärel püütakse 3. faasi uuringutes registreerida tuhandeid inimesi, et dokumenteerida tõhusus ja jätkata ohutusandmete vaatamist."
Oma veebisaidi andmetel on Pfizer oma uuringusse kaasanud üle 39 000 vabatahtliku. Neist enam kui 34 000 on saanud teise vaktsiiniannuse.
Mida see teie jaoks tähendab
3. faasi kliiniline uuring, mis hõlmab COVID-19 vaktsiini testimist lastel, on edasimineku märk. Vaktsiiniga ei saa aga kiirustada. Tulemuste lõplik vormistamine võtab aega, et kaitsta uuringus osalejate, samuti täiskasvanute ja laste ohutust, kes saavad lõpuks vaktsiini valmisversiooni.