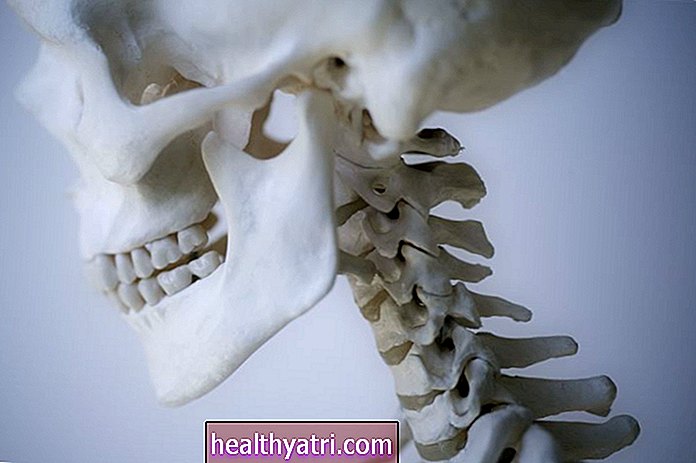
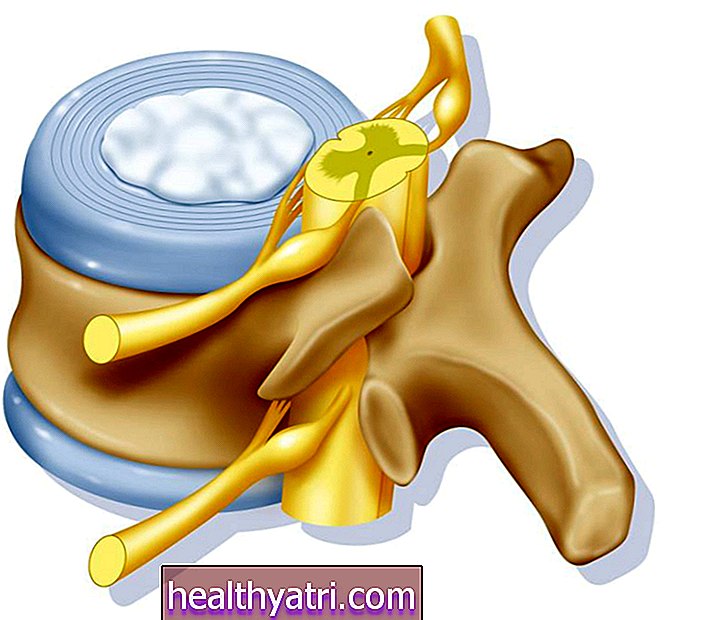
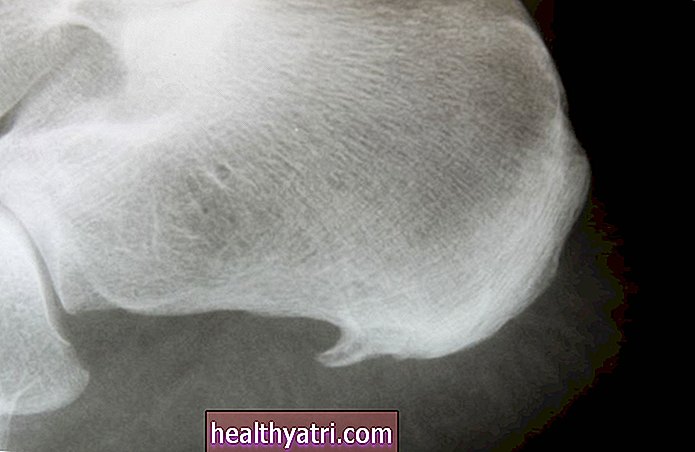
Emakaväline viitab objektile või inimese koele, mis moodustub või asub seal, kus see ei kuulu. Emakaväline luukoe moodustumine on uue luumaterjali ladumine (protsessiks, mida nimetatakse luustumiseks) piirkondades, kus see materjal ei kuulu. Selle luustumisprotsessi viivad läbi rakud, mida nimetatakse osteoblastideks.
Cecilie_Arcurs / Getty ImagesSõna emakaväline pärineb kreeklastelt ja tähendab "eemal kohast". Selle antonüüm, mis on “ortotoopne” luu - ka kreeka keelest tuletatud - viitab luule, mis on moodustatud õiges anatoomilises asukohas, väidavad Scott jt. al., oma artiklis pealkirjaga "Lühike ülevaade emakavälise luu moodustumise mudelitest". Artikkel ilmus ajakirja 2012. aasta märtsinumbris,Tüvirakkude areng.
Emakaväline luukoe moodustumine võib esineda sündides, olla tingitud geneetikast või tekkida teatud meditsiiniliste seisundite, näiteks parapleegia ja / või traumaatilise vigastuse komplikatsioonina (kui nimetada vaid mõnda). Scott jt. al. öelge, et emakavälise luukoe moodustumise põhjustab kohalik põletik, millele järgneb luustiku eellasrakkude kogunemine. Bostoni lastehaigla veebisaidi andmetel on eellasrakk sarnane tüvirakkudega, välja arvatud see, et see on piiratud rakutüüpide osas, mis võivad jagunemisel muutuda. Eellasrakud pärinevad tüvirakkudest, kuid ei ole täiskasvanud tüvirakud.
Lülisamba kirurgia tõttu emakaväline luukoe moodustumine
Scott jt. öelge, et kuni 10% -l invasiivse operatsiooni saavatest patsientidest - ja seljaoperatsioon kuulub kindlasti sellesse rühma - tekib emakaväline luukoe moodustumine.
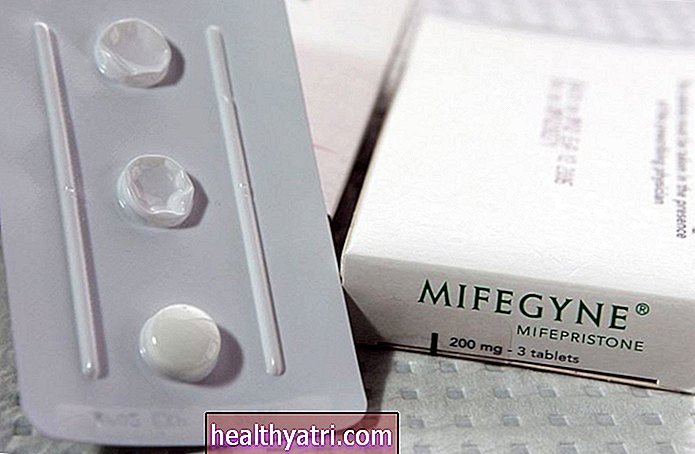
Selgroos kasutatakse mõnikord mõistet "emakaväline luukoe moodustumine" seljaaju kanalisse asetatud soovimatu luukoe kirjeldamiseks. 2002. aastal kiitis FDA heaks Medtronicu toodetud luuvalgu nimega Infuse, mis on ette nähtud lülisamba nimmeosa operatsioonides. FDA poolt määratletud kasutamiskriteeriumid olid väga spetsiifilised: luuülekandena ühetasandilise nimmepiirkonna esiosa vahekehade fusiooni (ALIF) jaoks nimmepiirkonna koonilise termotuumasünteesi seadme süsteemis (LT-Cage).
Kuid varsti pärast heakskiitmist hakkasid paljud kirurgid kasutama materjali "off-label", mis tähendab muul otstarbel kui FDA heakskiitu. Mitteväline kasutamine hõlmas lülisamba kaelaosa operatsiooni, mille tulemusel teatati FDA-le mitmetest kõrvaltoimetest või AE-st. Emakaväline luukoe moodustumine oli üks AE-sid, kuid loend hõlmas muid väga tõsiseid asju nagu arahnoidiit, suurenenud neuroloogiline defitsiit, retrograadne ejakulatsioon, vähk ja palju muud. Pole ilus.
Medtronicu poleemika
TheMilwaukee Journal SentinalValvekoera aruanne, mis on seda lugu jälginud alates 2011. aastast (ja jätkab seda ka edaspidi), ütleb, et nädalate jooksul pärast esimest Infuse kliinilist uuringut leiti 70% -l uuringu patsientidest emakaväline luukoe moodustumine. Mõned neist patsientidest vajasid soovimatu luu ja / või sellest tekkinud meditsiiniliste komplikatsioonide kõrvaldamiseks ühte või mitut operatsiooni.
2013. aasta väljaandes avaldatud tõendite ülevaatesOperatsioon Neuroloogia Rahvusvaheline, Võrdles Epstein 13 tööstusharust lähtuvat uuringut teiste hiljem ajakirjades avaldatud uuringutega, samuti FDA dokumentide ja andmebaasides sisalduva teabega. Ta teatab, et leidis Infuse uuringutega "algselt avaldamata kõrvaltoimeid ja sisemisi vastuolusid". Ta teatab ka, et 40% kõrvaltoimetest olid seotud ALIF-iga (nn kaelaoperatsioon, mis tehti), lisades, et mõned neist sündmustest olid eluohtlikud.
VahepealMilwaukee Journal Sentinelteatab, et Medtronic kas teatas neist kahjulikest mõjudest FDA-le kas üldse või ei teatanud neist üldse 2004. aasta aruandes, mille kirjutasid Medtronicu rahastatud arstid. MJSi sõnul saavad 2004. aasta töö kirjutanud arstid Medtronicult miljoneid dollareid autoritasusid ja muid makseid.
2014. aasta mais jätkas MJS seda lugu teise artikliga, milles öeldi, et Medtronic oli nõus maksma 22 miljonit dollarit, et rahuldada 1000 nõuet nende Infuse vastu. Selles loos mainiti ka seda, et Medtronic eraldab oodatavate nõuete katteks veel 140 miljonit dollarit.